TỔNG QUAN VỀ VIRUS EBV, CMV, HHV-6
Virus EBV
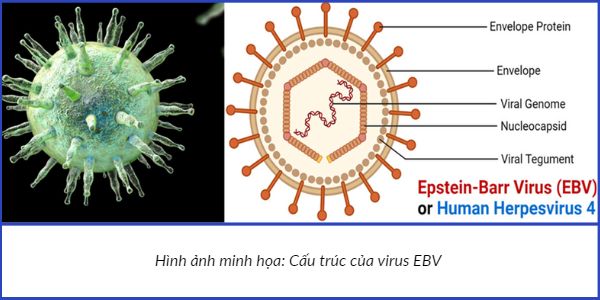
Epstein–Barr Virus (EBV) hay còn gọi là Herpesvirus-4, là một loại virus có khả năng gây ung thư thuộc họ virus Herpes. Virus EBV được phát hiện lần đầu tiên vào những năm 1960 trong các tế bào ung thư được phân lập từ khối u Burkitt [7].
Virus EBV có cấu tạo gồm 4 phần: một chuỗi DNA mạch kép được bao quanh bởi khối capsid đa diện; bên ngoài là lớp protein tegument và vỏ virus có gắn các glycoprotein đóng vai trò trong tính hướng và nhận dạng tế bào chủ của virus. Trung bình hạt virus trưởng thành có đường kính từ 122 đến 180nm [9]. Sau nhiễm trùng ban đầu, EBV tiềm ẩn trong nhóm tế bào B tuần hoàn của máu ngoại vi, giảm biểu hiện kháng nguyên để trốn tránh hệ thống miễn dịch. Vì vậy, nhiễm EBV nguyên phát thường không có triệu chứng. Trong quá trình tồn tại, virus có thể biểu hiện các protein tiềm ẩn hoặc ly giải như LMP1, EBNA1, v.v. biến đổi các thành phần trong cơ thể và có khả năng sinh ung thư [3].
Virus EBV dễ dàng lây truyền qua nước bọt bằng các hoạt động như hôn, dùng chung đồ dùng cá nhân như bàn chải đánh răng, dụng cụ ăn uống [10]. Ngoài ra, truyền máu và cấy ghép nội tạng cũng là con đường lây truyền virus [11]. Tỷ lệ lưu hành trên thế giới của virus EBV khác nhau phụ thuộc vào địa lý và độ tuổi. Tại Hoa Kỳ, trẻ em và thanh thiếu niên trong độ tuổi từ 6 đến 19 tuổi có tỷ lệ nhiễm EBV là 66,5% [2]. Ở Trung Quốc, một nghiên cứu cho thấy tỷ lệ EBV lớn hơn 50% trước 3 tuổi và hơn 90% ở độ tuổi từ 8 đến 9 tuổi [4].
Việc nhiễm virus có thể không có triệu chứng hoặc xảy ra những biến chứng nghiêm trọng như vỡ lách, viêm cơ tim, viêm não hoặc người bệnh mắc các loại ung thư như biểu mô vòm họng, ung thư biểu mô dạ dày, hội chứng Hodgkin, một số u lympho tế bào T và bệnh tăng sinh tế bào lympho sau ghép [1, 5, 6]. Người ta ước tính rằng hơn 250.000 trường hợp ung thư mỗi năm và khoảng 2% số ca ung thư tử vong do EBV gây ra [3].
Virus CMV
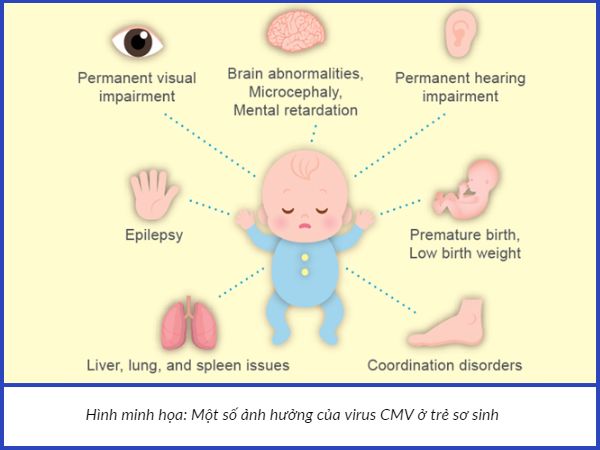
Cytomegalovirus (CMV) hay còn gọi là Herpesvirus-5, là một loại virus phổ biến thuộc họ virus Herpes. Mặc dù nhiễm CMV thường dẫn đến nhiễm trùng tiềm ẩn không có triệu chứng ở người khỏe mạnh, nhưng có khả năng gây bệnh tật và tử vong ở những bệnh nhân bị suy giảm miễn dịch [12, 13]. Đặc biệt ở trẻ sơ sinh, nhiễm CMV bẩm sinh từ mẹ trong thai kỳ hoặc chuyển dạ là nguyên nhân hàng đầu gây điếc không do di truyền. Ngoài ra, trẻ còn có khả năng chậm phát triển trí tuệ hoặc mất thị lực [14].
Với cấu trúc tương tự EBV, ngoài các thành phần cơ bản của virus, trên bề mặt vỏ của CMV có gắn glycoprotein giúp nhận dạng và xâm nhập vào tế bào chủ (tế bào niêm mạc, nguyên bào sợi, tế bào bạch cầu v.v.) [15, 16]. Con đường lan truyền chủ yếu của CMV qua các dịch cơ thể từ người nhiễm virus như nước bọt, nước mắt, sữa hoặc lây truyền dọc từ mẹ sang con trong quá trình mang thai hoặc chuyển dạ [14]. Tỉ lệ nhiễm virus CMV dao động từ 40-100% ở người trưởng thành, đối với trẻ sơ sinh, tỉ lệ này là 1%.
Sàng lọc CMV bẩm sinh để phát hiện phát hiện nguyên nhân mất thính giác để tiến hành điều trị sớm, cũng như theo dõi để can thiệp kịp thời ở những trường hợp khởi phát muộn [14].
Virus HHV-6
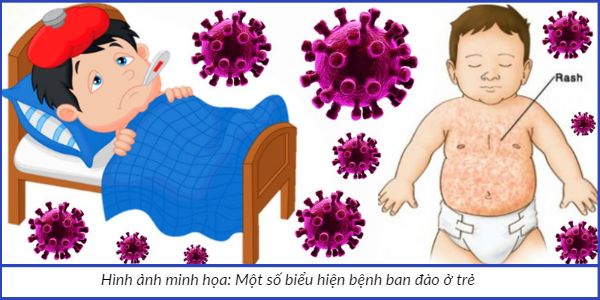
Virus Human Herpes-6 (HHV-6) là virus Herpes thứ 6 được phát hiện trong số 8 loại virus Herpes gây bệnh ở người, và được phân lập lần đầu vào năm 1986 ở bệnh nhân rối loạn tăng sinh tế bào lympho [17]. Hiện nay có hai biến thể của HHV-6: HHV-6A thường gây ảnh hưởng đối với người bị suy giảm miễn dịch; HHV-6B phổ biến hơn, là nguyên nhân của bệnh ban đào ở trẻ em [18].
HHV-6 có đường kính xấp xỉ 200 nm và có cấu trúc tương tự các virus Herpes khác. Loại virus này lây nhiễm nhiều loại tế bào ở người, nhưng chủ yếu thực hiện sao chép trong các tế bào lympho T - CD4. Nhiều nghiên cứu cho thấy có xảy ra sự tích hợp của bộ gen HHV-6 vào nhiễm sắc thể người. Sự sao chép của virus ảnh hưởng đến chức năng và sự tồn tại của tế bào chủ. Các protein của virus tạo môi trường vi mô thuận lợi cho virus hoạt động và trốn tránh miễn dịch của cơ thể [19].
Nhiễm HHV-6 ban đầu gây ra các triệu chứng như sốt, co giật, phát ban da và một số triệu chứng đường tiêu hóa và hô hấp ở trẻ nhỏ từ sáu tháng đến ba tuổi, điển hình nhất là bệnh sốt ban đào. Một số đường lây truyền của virus có thể kể đến như lây qua nước bọt hoặc cấy ghép tạng. Hơn 90% dân số thế giới từng nhiễm virus này [20].
XÉT NGHIỆM PHÁT HIỆN EBV/CMV/HHV-6
Ý Nghĩa Của Việc Xét Nghiệm
Như đã giới thiệu ở trên, nhiễm các virus EBV, CMV, HHV-6 liên quan tới nhiều loại bệnh lý nguy hiểm. Việc xét nghiệm phát hiện virus sớm, đặc biệt ở các đối tượng nguy cơ cao như bệnh nhân suy giảm miễn dịch, hoặc trẻ sơ sinh giúp đưa ra phương hướng điều trị kịp thời, giảm gánh nặng bệnh tật về sau.
Việc xét nghiệm virus EBV, CMV, HHV-6 thường dựa trên các kĩ thuật miễn dịch như định lượng kháng thể IgG, IgM kháng virus có trong huyết thanh, huyết tương người hoặc sử dụng kĩ thuật real-time PCR.
Xét Nghiệm EBV/CMV/HHV-6 Bằng Kĩ Thuật Real-Time PCR
Với ưu điểm độ nhạy, độ đặc hiệu cao và thời gian thực hiện nhanh chóng, Real-Time PCR là một trong những phương pháp thường được sử dụng để xét nghiệm EBV/CMV/HHV-6. DNA virus mục tiêu có trong mẫu lâm sàng sẽ được phát hiện nhờ mồi và đầu dò thiết kế đặc hiệu có gắn chất phát huỳnh quang. Kết quả khuếch đại DNA mục tiêu hiển thị trên màn hình ngay sau mỗi chu kỳ nhiệt của phản ứng.
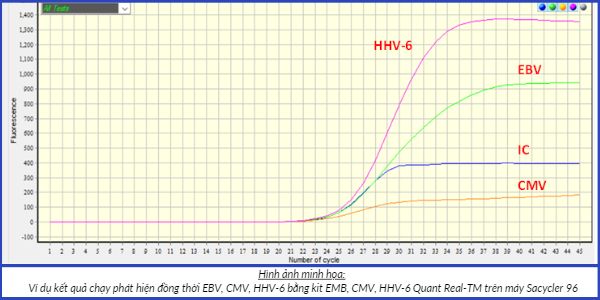
Bộ kit CMV/EBV/HHV6 Real-TM Quant dựa trên kỹ thuật Real-Time PCR,có thể phát hiện và định lượng đồng thời 3 tác nhân gây bệnh chỉ trong một ống phản ứng. Ngoài ra, trong phản ứng còn chứa mồi khuếch đại chứng nội (IC) là gen “giữ nhà” β-Globin, nhằm kiểm soát quá trình tách chiết và PCR. Bộ kit CMV/EBV/HHV6 Real-TM Quantcủa hãng Sacace (Ý), đạt tiêu chuẩn CE-IVD có thể chạy trên nhiều hệ máy Real-Time PCR khác nhau.
Việc phân tích kết quả đơn giản dựa vào tín hiệu trên 4 kênh màu: EBV được phát hiện trên kênh HEX, CMV trên kênh ROX, HHV-6 trên kênh Cy5 và chứng nội IC (β-Globin) trên kênh FAM. Độ nhạy của bộ kit cao: 400 copies/ ml đối với mẫu dịch não tủy và 5 DNA copies/ 105tế bào đối với mẫu máu toàn phần, tế bào bạch cầu hoặc mẫu sinh thiết.
Tài liệu tham khảo
[1] Odumade OA và cộng sự. Progress and problems in understanding and managing primary Epstein-Barr virus infections. Clin Microbiol Rev. 2011 Jan;24(1):193-209. Doi: 10.1128/CMR.00044-10.
[2] Dowd JB và cộng sự. Seroprevalence of Epstein-Barr virus infection in U.S. children ages 6-19, 2003-2010. PLoSOne. 2013;8(5):e64921. Doi: 10.1371/journal.pone.0064921.
[3] Yu H và cộng sự. 2023. Epstein–Barr Virus History and Pathogenesis. Viruses 15, no. 3: 714. https://doi.org/10.3390/v15030714
[4] Xiong G và cộng sự. Epstein-Barr virus (EBV) infection in Chinese children: a retrospective study of age-specific prevalence. PLoS One. 2014;9(6):e99857. Doi: 10.1371/journal.pone.0099857.
[5] Watanabe M và cộng sự. Acute Epstein-Barr related myocarditis: An unusual but life-threatening disease in an immunocompetent patient. J Cardiol Cases. 2020 Apr;21(4):137-140. Doi: 10.1016/j.jccase.2019.12.001.
[6] Mărginean MO và cộng sự. Epstein-Barr virus-associated hemophagocytic lymphohistiocytosis in a small child: A case report. Medicine (Baltimore). 2020 Jan;99(3):e18759. Doi: 10.1097/MD.0000000000018759.
[7] Epstein, M. A và cộng sự. 1964. Virus particles in cultured lymphoblasts from Burkitt's lymphoma. Lancet i:702-703. Doi: 10.1016/s0140-6736(64)91524-7.
[9] Thompson MP và cộng sự. Epstein-Barr virus and cancer. Clin Cancer Res (2004) 10(3):803–21. 10.1158/1078-0432.CCR-0670-3. Doi: 10.1158/1078-0432.ccr-0670-3
[10] Maria K. Smatti và cộng sự. Epstein–Barr Virus Epidemiology, Serology, and Genetic Variability of LMP-1 Oncogene Among Healthy Population: An Update. Front Oncol. 2018; 8: 211. Doi: 10.3389/fonc.2018.00211.
[11] Alfieri C và cộng sự. Epstein-Barr virus transmission from a blood donor to an organ transplant recipient with recovery of the same virus strain from the recipient’s blood and oropharynx. Blood (1996) 87(2):812–7. Doi: 10.1182/blood.V87.2.812.bloodjournal872812
[12] Rafailidis P.I và cộng sự. Severe cytomegalovirus infection in apparently immunocompetent patients: a systematic review. Virol. J. 2008; 5: 47. Doi: doi:10.1186/1743-422X-5-47
[13] Coaquette A và cộng sự. Mixed cytomegalovirus glycoprotein B genotypes in immunocompromised patients, Clin. Infect. Dis. 2004; 39: 155-161. Doi: 10.1086/421496
[14] Maggie Kettler và cộng sự. American Academy of Audiology Position Statement on Early Identification of Cytomegalovirus in Newborns. 2023. American Academy of Audiology. Doi: 10.1055/s-0043-1768036.
[15] Susan M. Varnum và cộng sự. Identification of Proteins in Human Cytomegalovirus (HCMV) Particles: the HCMV Proteome. J Virol. 2004 Oct; 78(20): 10960–10966. Doi: 10.1128/JVI.78.20.10960-10966.2004
[16] Paul Griffith và cộng sự. Pathogenesis of human cytomegalovirus in the immunocompromised host. (2021) Nature Reviews Microbiology 19, 759–773. Doi: 10.1038/s41579-021-00582-z
[17] Salahuddin SZ và cộng sự. Isolation of a new virus, HBLV, in patients with lympho-proliferative disorders (1986). Science 234:596–601. Doi: 10.1126/science.2876520.
[18] Ablashi D và cộng sự. Classification of HHV-6A andHHV-6B as distinct viruses. (2014). Arch Virol 159:863–870. Doi: 10.1007/s00705-013-1902-5
[19] Agut H và cộng sự. Humanherpesviruses 6A, 6B, and 7. 2016. Microbiol Spectrum 4(3):DMIH2-0007-2015. Doi: 10.1128/microbiolspec.DMIH2-0007-2015.
[20] Yamanishi K và cộng sự. Identification of human herpesvirus-6 as a causal agent for exanthem subitum. Lancet 1988, 1, 1065–1067. Doi: 10.1016/s0140-6736(88)91893-4









 ĐKKD:
ĐKKD: 
